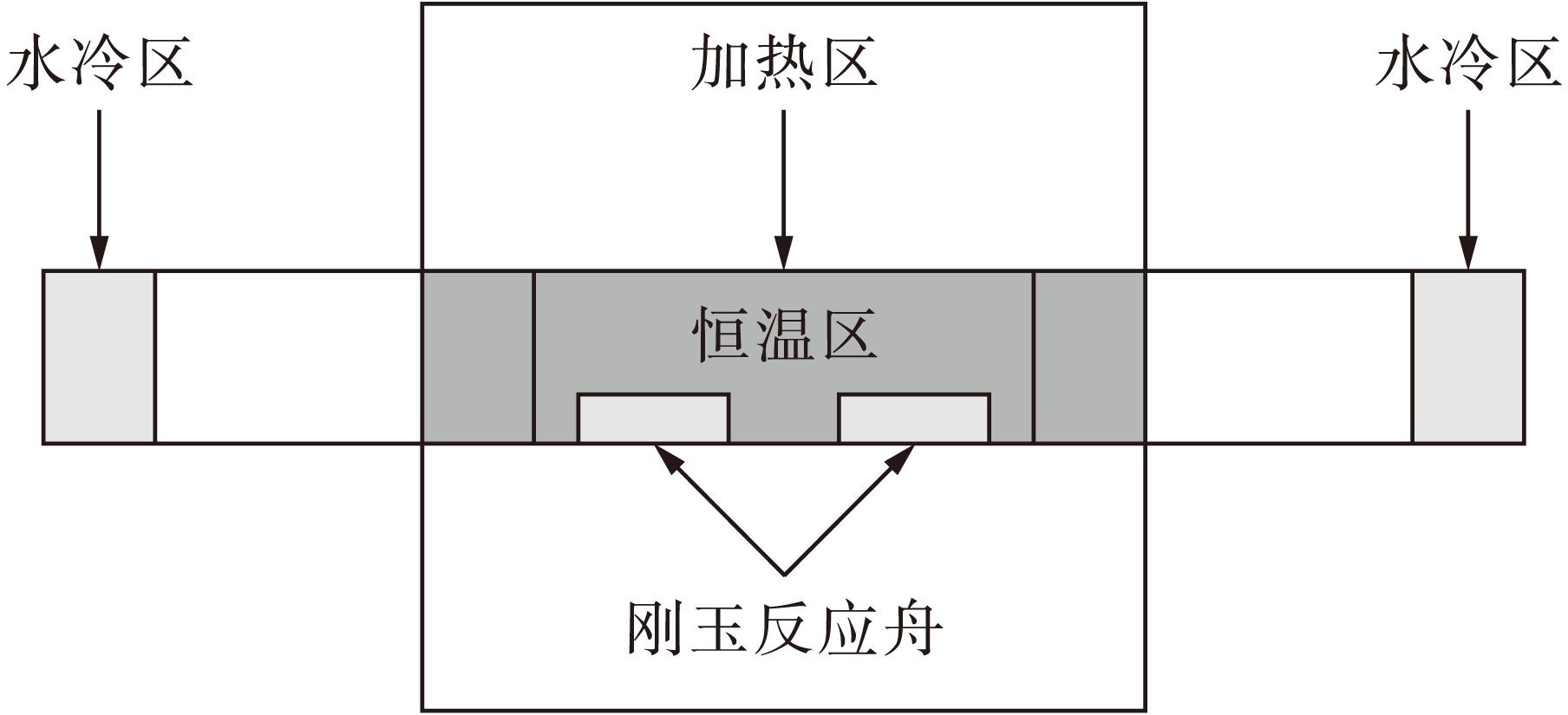
图1 管式烧结炉示意图
Fig.1 Schematic diagram of tube sintering furnace
李志杰, 张玉峰, 吴 霄
(沈阳工业大学 理学院, 沈阳 110870)
摘 要:为了提高SrAl2O4∶Eu2+,Dy3+荧光材料的发光强度和余辉时间,采用高温固相法合成了SrAl2O4∶Eu2+,Dy3+荧光粉.利用X射线衍射仪、扫描电子显微镜和荧光光谱仪对产物的化学成份、结构、微观形貌和发光特性进行了分析.结果表明,SrAl2O4∶Eu2+,Dy3+荧光粉的最佳煅烧温度为1 500 ℃,最佳煅烧时间为3 h.当Eu2O3的质量分数为2%时,SrAl2O4∶Eu2+荧光粉的发光强度最大;当Eu2O3的质量分数为1.5%时,SrAl2O4∶Eu2+荧光粉的余辉性能最好;当Eu2O3的质量分数为2%、Dy2O3的质量分数为4%时,SrAl2O4∶Eu2+,Dy3+荧光粉的发光强度和余辉性能最好.
关 键 词:荧光材料; 发光强度; 最佳煅烧温度; 高温固相法; 微米粉; 发射谱; 余辉; 合成
90年代以来,以MAl2O4:Eu2+(M=Ca,Sr,Ba)为代表的稀土离子掺杂碱土铝酸盐长余辉发光材料,开辟了长余辉稀土发光材料的新篇章[1-4].稀土Eu2+激活铝酸盐发光材料是以碱土铝酸盐为基质,并掺入Eu2+作为激活剂.由于Eu2+可与基质离子间发生有效的能量传递,当发光材料受紫外光或近紫外可见光照射时,碱土铝酸盐基质会将吸收的光能传递给掺入晶格的Eu2+,并使之受激而发光.Matsuzawa[5]在1996年首次将Dy元素作为辅助激活剂掺入铝酸锶中,提升了其发光强度和余辉时间,拓宽了其应用领域.Eu2+、Dy3+共掺杂的碱土铝酸盐系列发光材料,是目前已知的长余辉发光性能最好的蓄光型发光材料.该发光材料具有发光效率高、余辉时间长、化学性能稳定与无放射性危害等优点,因而有望成为一类新型高效稳定的发光材料[6-8].
目前,有关以碱土铝酸盐为基底的系列发光材料的研究多集中在粉体多晶和块体单晶方面.制备方法主要包括高温固相法[9-11]、燃烧法、微波合成法、共沉淀法和溶胶-凝胶法,其中高温固相法是工业生产中应用最多的方法.1995年,宋庆梅[12]等在原有研究的基础上经过一系列实验,得到了掺杂镁且余辉强度更强的SrAl2O4∶Eu2+磷光体,其余辉衰减呈双曲线型,同时发现掺钙的SrAl2O4∶Eu2+荧光粉无任何长余辉发光效应.不同的烧结温度,会对晶相产生不同的影响.Douy[13]等在制备Sr4Al14O25产物过程中,对产物的晶相进行了检测分析后发现,在不同温度下,产物可以形成不同的晶相;在1 300 ℃下烧结数小时后,可以得到单一相的Sr4Al14O25产物.原料成分的不同,也会对产物性能产生一定的影响.胡劲[14]等采用活化铝锶合金粉末,制备了SrAl2O4长余辉材料的前驱体后发现,在微观状态下,前驱体中Sr、Al元素均匀分布;当采用固相法合成SrAl2O4∶Eu2+,Dy3+长余辉材料时,所得产物的发光性能较好.
1.1 主要原料
实验所用主要原料包括产自国药集团化学试剂有限公司的碳酸锶(SrCO3)、氧化铕(Eu2O3)和氧化镝(Dy2O3),以及产自沈阳市试剂三厂的氧化铝(Al2O3).
1.2 SrAl2O4∶Eu2+,Dy3+荧光粉的合成
将各组分按照一定比例进行称量后放入烧杯中,掺入定量的氧化铕和氧化镝,加入适量的酒精使原料溶解.边搅拌边进行水浴加热,直至原料干燥为止.将干燥后的原料充分研磨后放入刚玉反应舟内,并置于管式烧结炉加热区中央,管式烧结炉示意图如图1所示.在恒温加热过程中利用热电偶测试相应温度.炉腔抽真空至2×10-4Pa为止,再充入H2与Ar的混合气体(体积分数分别为5%和95%).在实验过程中,需要在1 h内快速升温至相应温度.经过不同时间的恒温处理后结束加热,自然冷却至室温后取出产物.在反应过程中涉及到的主要化学反应为
SrCO3→SrO+CO2
Al2O3+SrO→SrAl2O4
SrAl2O4+Eu2++Dy3+→SrAl2O4∶Eu2+,Dy3+

图1 管式烧结炉示意图
Fig.1 Schematic diagram of tube sintering furnace
1.3 测试与表征
利用产自中国天桥仪器设备有限责任公司的BDX3200型X射线衍射仪与产自日本电子株式会社的JSM-6301F型场发射扫描电子显微镜,对SrAl2O4∶Eu2+,Dy3+荧光粉的物相结构及微观形貌进行了表征.利用产自日本日立公司的F-4500型荧光分光光度计,对SrAl2O4∶Eu2+,Dy3+荧光粉的发光性能进行了测试.
2.1 煅烧温度和煅烧时间
图2为相同原料在不同温度煅烧3 h后所得产物的XRD图谱.将图2a与相应PDF卡片对比后可以发现,![]() 11)、(220)、(211)与(031)晶面处为单斜结构SrAl2O4(JCPDS No.34-0379)的特征峰,(440)、(800)晶面处为立方结构Sr3Al2O6(JCPDS No.24-1187)的特征峰.此外,在图2a中未发现其他明显特征峰的存在.对比图2a、b后可知,当煅烧温度由1 300 ℃升高到1 400 ℃时,相对于SrAl2O4而言,Sr3Al2O6的特征峰强度明显降低,表明当煅烧温度从1 300 ℃升高到1 400 ℃时,Sr3Al2O6生成量降低,而SrAl2O4生成量增多.当温度继续升高到1 500 ℃时,Sr3Al2O6在(800)晶面处的特征峰已经消失,而在(440)晶面处的特征峰强度也随着温度的升高而大幅度降低.由图2还可以观察到,Sr3Al2O6为反应的中间产物,提高反应温度能使其含量明显减少.然而,当煅烧温度超过1 500 ℃时,所得产物的发光强度和余辉时间将会急剧下降,因此,制备荧光粉的最佳煅烧温度为1 500 ℃.
11)、(220)、(211)与(031)晶面处为单斜结构SrAl2O4(JCPDS No.34-0379)的特征峰,(440)、(800)晶面处为立方结构Sr3Al2O6(JCPDS No.24-1187)的特征峰.此外,在图2a中未发现其他明显特征峰的存在.对比图2a、b后可知,当煅烧温度由1 300 ℃升高到1 400 ℃时,相对于SrAl2O4而言,Sr3Al2O6的特征峰强度明显降低,表明当煅烧温度从1 300 ℃升高到1 400 ℃时,Sr3Al2O6生成量降低,而SrAl2O4生成量增多.当温度继续升高到1 500 ℃时,Sr3Al2O6在(800)晶面处的特征峰已经消失,而在(440)晶面处的特征峰强度也随着温度的升高而大幅度降低.由图2还可以观察到,Sr3Al2O6为反应的中间产物,提高反应温度能使其含量明显减少.然而,当煅烧温度超过1 500 ℃时,所得产物的发光强度和余辉时间将会急剧下降,因此,制备荧光粉的最佳煅烧温度为1 500 ℃.
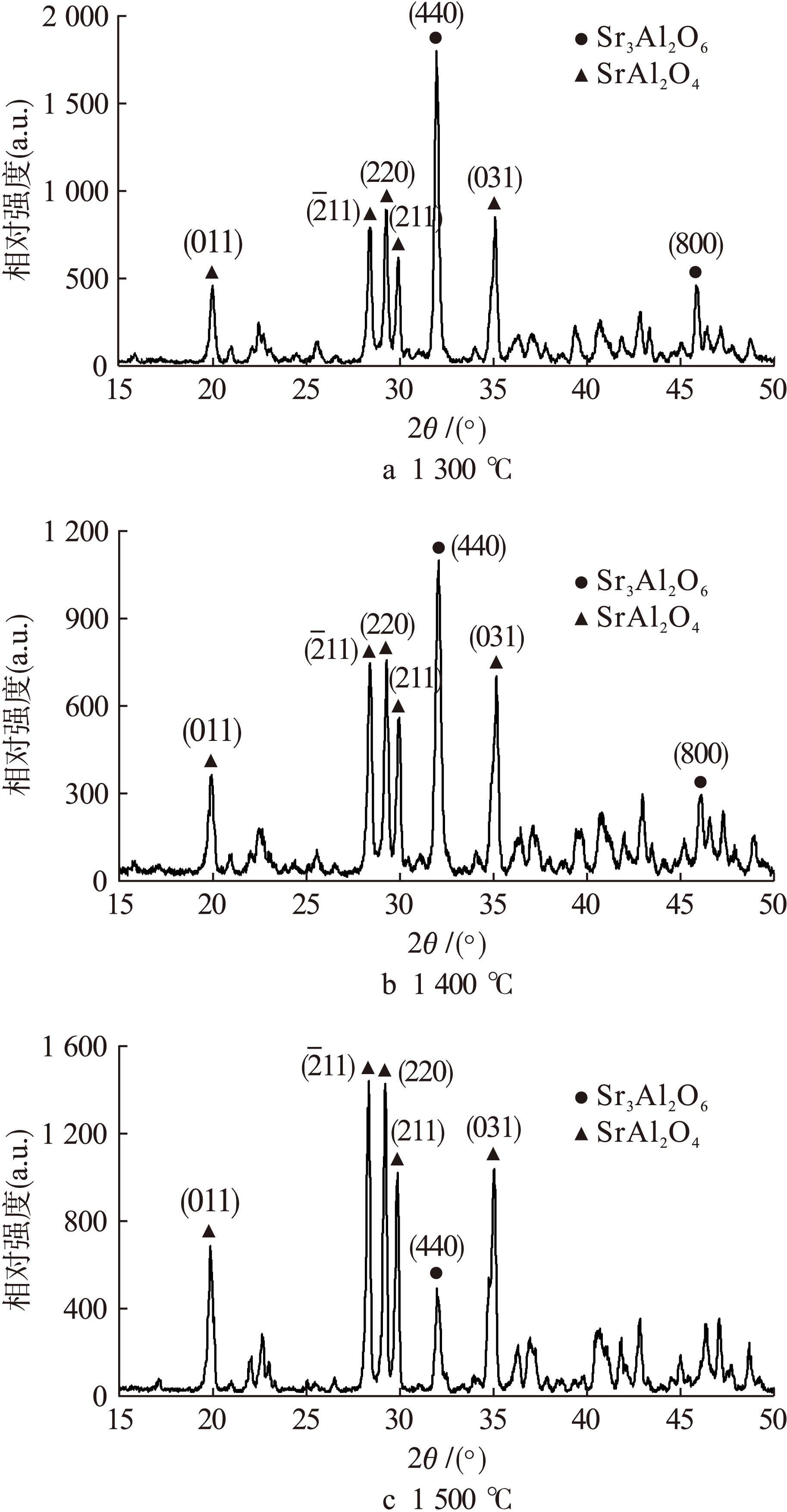
图2 不同煅烧温度下产物的XRD图谱
Fig.2 XRD spectra of products with different calcination temperatures
图3为相同原料在1 500 ℃煅烧不同时间后所得产物的发射谱.利用波长为365 nm的紫外光,可以激发得到特征峰的发射谱.图3中的发射谱特征峰对应于Eu2+在SrAl2O4单斜结构中的发光特征峰,发光颜色为黄绿色.粉体材料发射谱特征峰对应的块体,在520 nm处呈现微弱的蓝移现象.可以认为,随着产物粒径的减小,电子动能增大,导致能带中4f能级到5d能级之间的距离增大,因此,发射谱特征峰发生了微弱蓝移.由图3可见,当煅烧时间为1 h时,产物的发光强度最差.随着煅烧时间的增加,产物的发光强度迅速提高,当煅烧时间为3 h时,产物的发光强度最高.当煅烧时间达到4 h时,发光强度开始变差,表明过长时间的煅烧会降低产物的发光性能,因此,制备荧光粉的最佳煅烧时间为3 h.
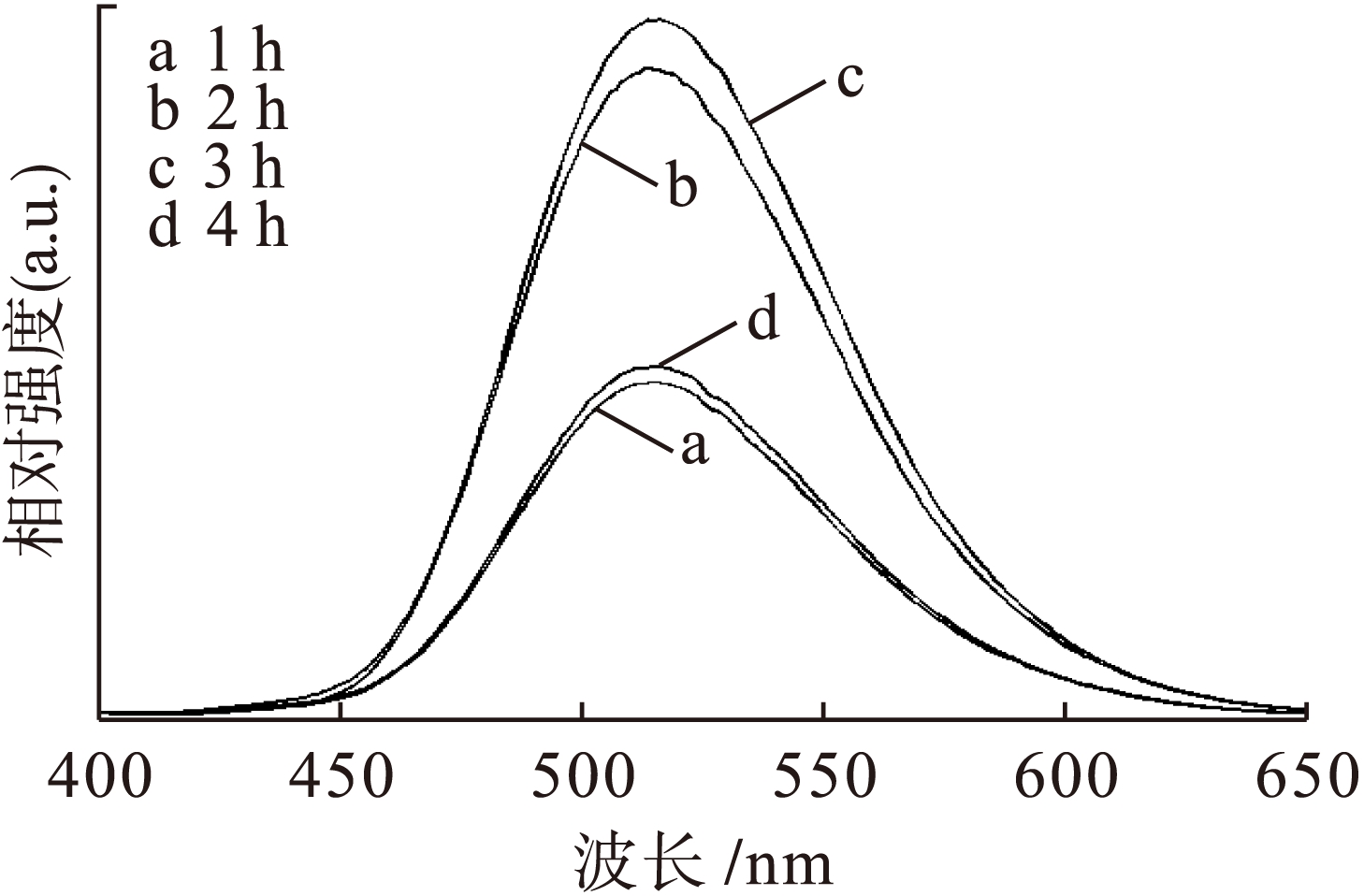
图3 不同煅烧时间下产物的发射谱
Fig.3 Emission spectra of products with different calcination time
2.2 氧化铕掺杂量
图4和图5分别为含有不同氧化铕掺杂量的SrAl2O4在1 500 ℃下煅烧3 h后,所得产物SrAl2O4∶Eu2+的发射谱和余辉曲线.由图4可见,随着氧化铕掺杂量(质量分数)的增加,产物的发光强度先增大后减小.具体而言,当氧化铕的质量分数由0.5%提高到2%时,产物的发光强度随着氧化铕掺杂量的增加而增大.当氧化铕的质量分数为2%时,产物的发光强度达到最大值.当继续增加氧化铕的掺杂量,使其质量分数达到3%时,产物的发光强度显著降低.因此,为了使产物具有最佳的发光强度,氧化铕的质量分数应为2%.由图5可知,随着氧化铕掺杂量的增多,产物的余辉性能也呈现出先增大后减小的规律.当氧化铕的质量分数由0.5%提高到1.5%时,产物的余辉性能随着氧化铕掺杂量的增加而增大.当氧化铕的质量分数为1.5%时,产物的余辉性能达到最大值.当继续增加氧化铕的掺杂量,使其质量分数达到3%时,产物的余辉性能显著降低.因此,为了使产物具有最好的余辉性能,氧化铕的质量分数应为1.5%.

图4 SrAl2O4∶Eu2+的发射谱
Fig.4 Emission spectra of SrAl2O4∶Eu2+
2.3 氧化镝掺杂量
图6和图7为同时掺杂了质量分数为2%的氧化铕与不同含量氧化镝的SrAl2O4,在1 500 ℃煅烧3 h后,所得产物SrAl2O4∶Eu2+,Dy3+的发射谱和余辉曲线.由图6和图7可以看出,产物的发光强度和余辉性能均随着氧化镝质量分数的增加先增加后减少.因此,当氧化铕的质量分数为2%、氧化镝的质量分数为4%时,产物的整体性能最佳.
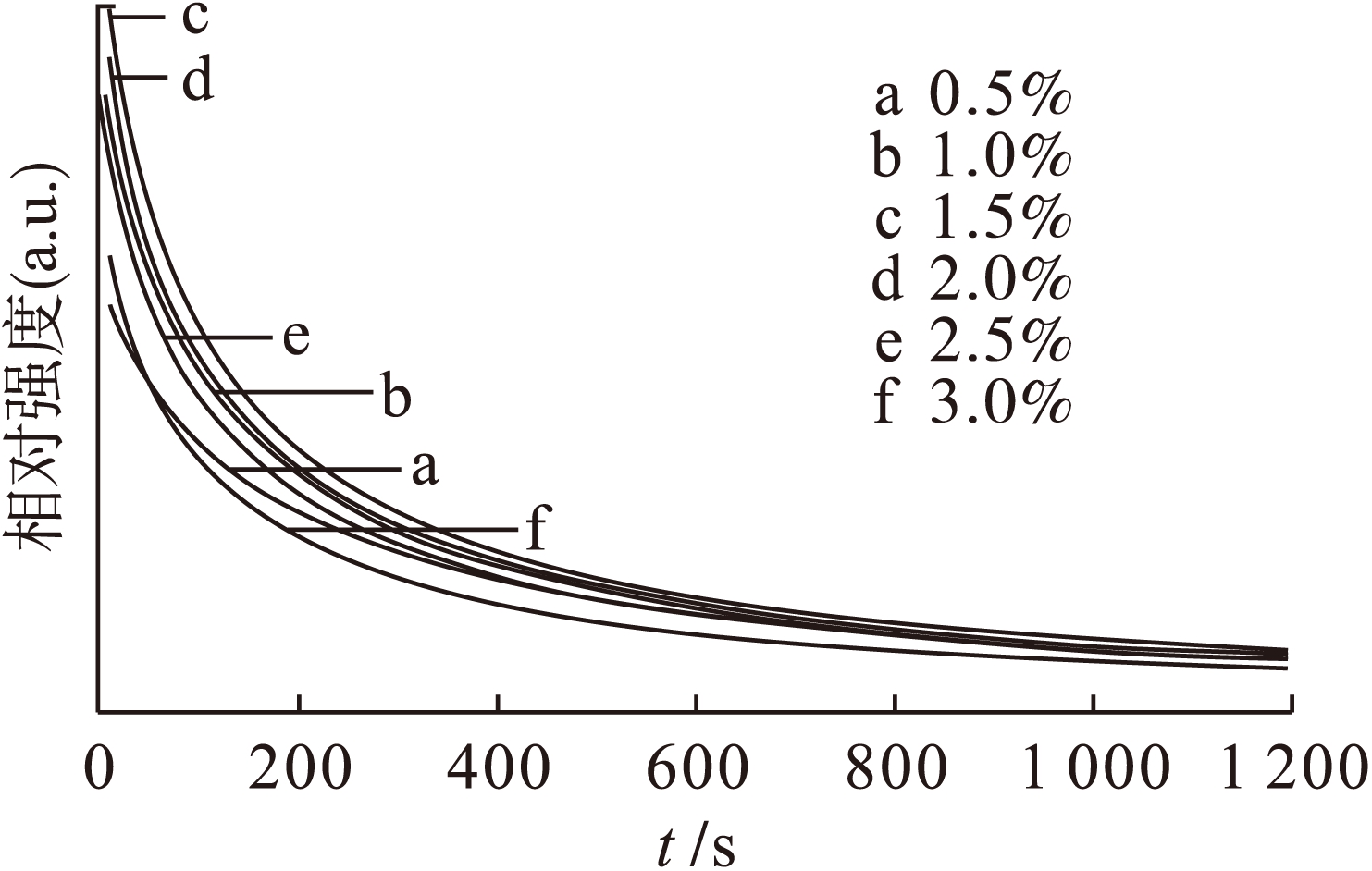
图5 SrAl2O4∶Eu2+的余辉曲线
Fig.5 Afterglow curves for SrAl2O4∶Eu2+
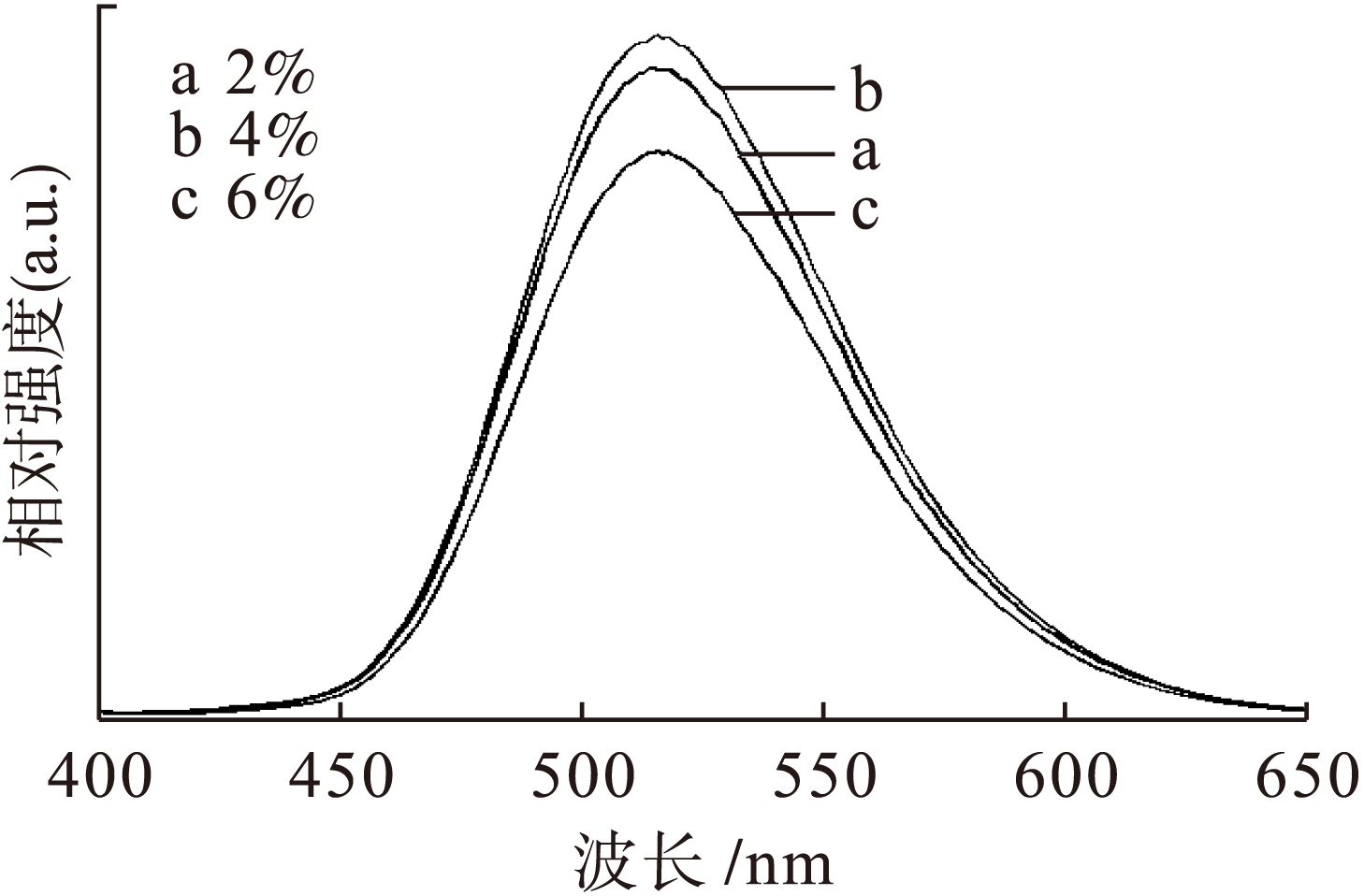
图6 SrAl2O4∶Eu2+,Dy3+的发射谱
Fig.6 Emission spectra of SrAl2O4∶Eu2+,Dy3+

图7 SrAl2O4∶Eu2+,Dy3+的余辉曲线
Fig.7 Afterglow curves for SrAl2O4∶Eu2+,Dy3+
2.4 SEM分析与EDS图谱
图8为不同煅烧温度下SrAl2O4∶Eu2+,Dy3+的SEM图像.由图8可见,随着煅烧温度的升高,产物颗粒直径由1 300 ℃下的0.5 μm增加到1 500 ℃下的1 μm,且其致密性也存在明显的提高,这是产物发光性能提升的一个重要原因.
图9和图10分别为掺杂了质量分数为2%的氧化铕与质量分数为4%的氧化镝的SrAl2O4,在1 500 ℃煅烧3 h后所得产物的SEM图像与EDS图谱.由图9可见,所得产物是一种微米级的粉体,其表面形态并不规则,且存在团聚现象.图10为图9方框区域的能谱图像.由图10可见,Al、Sr的原子分数比接近于2∶1,可从侧面证明所制备的荧光粉为SrAl2O4.

图8 不同煅烧温度下SrAl2O4∶Eu2+,Dy3+的SEM图像
Fig.8 SEM images of SrAl2O4∶Eu2+,Dy3+with different calcination temperatures

图9 SrAl2O4∶Eu2+,Dy3+的SEM图像
Fig.9 SEM image of SrAl2O4∶Eu2+,Dy3+

图10 SrAl2O4∶Eu2+,Dy3+的EDS图谱
Fig.10 EDS spectrum of SrAl2O4∶Eu2+,Dy3+
通过以上实验分析,可以得到如下结论:
1) 合成SrAl2O4∶Eu2+,Dy3+荧光粉的最佳煅烧温度为1 500 ℃,最佳煅烧时间为3 h.当煅烧温度较低、煅烧时间较短时,反应不充分,生成产物多为具有立方结构的Sr3Al2O6;当煅烧温度过高、煅烧时间过长时,则会降低产物的发光强度和余辉性能.
2) 当合成SrAl2O4∶Eu2+荧光粉时,随着氧化铕掺杂量的增多,产物的发光强度和余辉性能均先增强后减弱.当氧化铕的质量分数为2%时,产物的发光强度最佳;当氧化铕的质量分数为1.5%时,产物的余辉性能最佳.
3) 当合成SrAl2O4∶Eu2+,Dy3+荧光粉时,随着氧化镝掺杂量的增多,产物的发光强度和余辉性能也呈现先增强后减弱的规律.当氧化镝的质量分数4%时,产物的发光强度和余辉性能均最佳.
参考文献(References):
[1]Peng X,Li S X,Liu X J,et al.Syntheses and photoluminescence properties of Eu2+/Tb3+doped Sr2Si5N8phosphors [J].Journal of Inorganic Materials,2015,30(4):397-400.
[2]Qin J L,Zhang H R,Lei B F,et al.Thermolumine-scence and temperature-dependent afterglow properties in BaSi2O2N2∶Eu2+[J].Journal of the American Ceramic Society,2013,96(10):3149-3154.
[3]Zhang H R,Lei B F,Qin J L,et al.Preparation of SrSi2O2N2∶Eu2+phosphor by SrSi alloy precursor and its long-lasting phosphorescence properties [J].Journal of the American Ceramic Society,2013,96(6):1810-1814.
[4]滕瑞,李金国,刘纪德,等.终烧温度对陶瓷型芯性能的作用 [J].沈阳工业大学学报,2014,36(1):23-27.
(TENG Rui,LI Jin-guo,LIU Ji-de,et al.Effect of sintering temperature on performance of ceramic mold core [J].Journal of Shenyang University of Techno-logy,2014,36(1):23-27.)
[5]Matsuzawa T,Aoki Y.A new long phosphorescent phosphor with high brightness SrAl2O4∶Eu2+,Dy3+[J].Journal of the Electrochemical Society,1996,143(8):2670-2673.
[6]Komatsu K,Tsuchida S,Maruyama H,et al.Synthesis of a violet Sr-Al-O∶Eu2+phosphor particle using elemental Al diffusion [J].International Journal of Applied Ceramic Technology,2014,11(3):594-601.
[7]Xue Z P,Deng S Q,Liu Y L.Synthesis and lumine-scence properties of SrAl2O4∶Eu2+,Dy3+nanosheets [J].Physica B,2012,407(18):3808-3812.
[8]Bulur E,Gksu H Y,Wieser A,et al.Thermolumine-scence properties of fluorescent materials used in commercial lamps [J].Radiation Protection Dosimetry,1996,65(1):373-379.
[9]Xie W,Wang Y H,Hu Y H,et al.Structure and luminescence properties of Sr4Al14O25∶Eu2+,Dy3+by Ba2+substitution [J].Rare Metal Materials and Engineering,2011,40(5):921-926.
[10]Xie W,Wang Y H,Hu Y H,et al.Structure and luminescence properties of Sr4Al14O25∶Eu2+,Dy3+by Ca2+doping [J].Acta Physica Sinica,2010,59(2):1148-1154.
[11]Feng X,Feng W L,Wang K.Experimental and theore-tical spectroscopic study of praseodymium(Ⅲ) doped strontium aluminate phosphors [J].Journal of Alloys & Compounds,2015,628(4):343-346.
[12]宋庆梅,陈暨耀,吴中亚.掺镁的铝酸锶铕磷光体的发光特性 [J].复旦大学学报(自然科学版),1995,34(1):103-106.
(SONG Qing-mei,CHEN Ji-yao,WU Zhong-ya.A study on luminescence of Mg doped SrAl2O4∶Eu phosphor [J].Journal of Fudan University (Natural Science),1995,34(1):103-106.)
[13]Douy A,Capron M.Crystallisation of spray-dried amorphous precursors in the SrO-Al2O3system:a DSC study [J].Journal of the European Ceramic Society,2003,23(12):2075-2089.
[14]胡劲,孙家林,刘建良,等.Eu,Dy共掺杂SrAl2O4长余辉材料制备新工艺 [J].发光学报,2006,27(2):179-182.
(HU Jin,SUN Jia-lin,LIU Jian-liang,et al.New pre-paration process of long afterglow phosphor Eu and Dy codoped SrAl2O4[J].Chinese Journal of Lumine-scence,2006,27(2):179-182.)
(责任编辑:尹淑英 英文审校:尹淑英)
LI Zhi-jie, ZHANG Yu-feng, WU Xiao
(School of Science, Shenyang University of Technology, Shenyang 110870, China)
Abstract:In order to improve the luminescence intensity and afterglow time of SrAl2O4∶Eu2+, Dy3+fluorescent material, the SrAl2O4∶Eu2+, Dy3+fluorescent powder was synthesized with high temperature solid state method. The chemical composition, structure, microscopic morphology and luminescent properties of products were analyzed with X ray diffractometer (XRD), scanning electron microscope (SEM) and fluorescence spectrometer. The results show that the optimum calcination temperature of SrAl2O4∶Eu2+, Dy3+fluorescent powder is 1 500 ℃, and the optimum calcination time is 3 h. When the mass fraction of Eu2O3is 2%, the SrAl2O4∶Eu2+fluorescent powder has the maximum luminescence intensity. When the mass fraction of Eu2O3is 1.5%, the SrAl2O4∶Eu2+fluorescent powder has the best afterglow performance. When the mass fraction of Eu2O3is 2% and the mass fraction of Dy2O3is 4%, the SrAl2O4∶Eu2+, Dy3+luorescent powder has the best luminescence intensity and afterglow performance.
Key words:fluorescence material; luminescence intensity; optimum calcination temperature; high temperature solid state method; micron powder; emission spectrum; afterglow; synthesis
收稿日期:2015-12-01.
基金项目:国家自然科学基金资助项目(21571132); 辽宁省科学技术计划项目(2012222010).
作者简介:李志杰(1963-),男,辽宁沈阳人,教授,博士,主要从事纳米材料制备、应用及发光材料等方面的研究.
材料科学与工程
doi:10.7688/j.issn.1000-1646.2016.05.01
中图分类号:TB 381
文献标志码:A
文章编号:1000-1646(2016)05-0481-05
*本文已于2016-05-12 14∶01在中国知网优先数字出版. 网络出版地址:http:∥www.cnki.net/kcms/detail/21.1189.T.20160512.1401.036.html